- 首页 > 正文
对付耐药,有依可靠!卓超、施毅、郑波教授分享CRO治疗的研究进展和诊疗经验
感染医线 发表时间:2023/4/12 21:04:07
编者按:耐药细菌尤其是广泛耐药的革兰阴性菌(MDR-GNB)、碳青霉烯类耐药革兰阴性杆菌(CRO)是悬在人类头顶的“达摩克利斯之剑”,每年全球导致120多万的死亡病例[1]。除了强调耐药细菌的连续监测、临床快速诊断、抗菌药合理应用以外,临床医生最为关注的是手里是否有足够强效的治疗“武器”。近期,全球首个新型、广谱、全合成含氟四环素抗菌药依拉环素获得国家药品监督管理局(NMPA)批准上市许可申请,将与中国医生和患者共同迎战耐药细菌的挑战。
在近日举行的中华医学会第三次全国细菌真菌感染学术会议(BISC 2023)上,《感染医线》邀请广州医科大学附属第一医院卓超教授、南京大学医学院附属金陵医院施毅教授、北京大学第一医院郑波教授,一起分享耐药细菌尤其是CRO的研究进展和诊疗经验。三位专家分别从集中带量采购(VBP)下的抗菌药合理应用、重症监护室(ICU)耐药菌感染的经验性治疗、抗菌药联合治疗常见CRO感染等角度,剖析依拉环素的上市可及,将对临床实践产生的影响。
点击上方链接查看采访视频

卓超 教授
集采大势下的抗菌药合理应用
新药上市破解耐药难题
从2018年第一批集采以来,国家启动了八批次的集采,大约有51个抗菌药品种被纳入其中。卓超教授指出,尽管集采明显降低了医疗费用,但也带来了新的临床问题。首先是部分医生对药品“质量”的担忧,虽然纳入集采的仿制药通过了一致性评价,但目前我们仍缺乏基于临床的综合评价数据和体系,且仍有不少患者有原研药、创新药的治疗需求。其次是对“存量”过剩的担忧,大量采购的同时面临着怎样消耗存量的问题,而临床用药的原则应该是“按需使用”的。
需要警惕的是,集采对抗菌药合理应用的潜在影响。在降价驱动下,纳入集采的药品使用量会增加,导致某类抗菌药使用强度(DDD)的增加,从而诱导该院或该地区的细菌耐药产生。国家政策也在调整,将逐渐建立以临床需求为导向的集采,未来也需要更多来自真实世界的数据提供信息。
卓超教授认为,抗菌药的合理应用需要破除“唯价格论”,而且离不开创新药物为临床“注入新鲜血液”。在全球耐药菌感染发病率上升的形势下,临床医生非常关心的是手里是否有强效的“武器”,尤其是应对碳青霉烯类耐药革兰阴性杆菌(CRO)这类治疗选择非常有限的耐药菌。近年来,CRO成为全球关注的焦点,尤其是碳青霉烯类耐药鲍曼不动杆菌(CRAB)、碳青霉烯类耐药铜绿假单胞菌(CRPA)、碳青霉烯类耐药肠杆菌科(CRE)被WHO列入抗菌药开发最优先级别(极为迫切)。目前,临床上可用于CRO治疗的抗菌药十分有限。有的药物存在安全性问题,有的药物也面临耐药风险。例如,IDSA指南将头孢他啶-阿维巴坦作为CRO治疗的推荐之一,但也指出头孢他啶-阿维巴坦暴露后相对其他药物更容易产生耐药[2]。某类药物的使用频率太高也会加剧耐药风险,因此需要强调抗菌药选择的多元化,鼓励创新药物的加入,从而延缓耐药进展。
依拉环素是一种新型的全合成含氟四环素。作为第三代四环素类药物,替加环素国内上市十余年以来,临床使用频率明显增加,不少地区出现了替加环素耐药菌增加的情况。卓超教授表示,我们希望有更多依拉环素此类新药上市,为临床提供更优化、更多元化的选择。依拉环素的抗菌谱非常广,可以覆盖除铜绿假单胞菌以外的革兰阴性菌、革兰阳性菌、厌氧菌、非典型菌,包括肺炎克雷伯菌、鲍曼不动杆菌、大肠埃希菌等常见革兰阴性菌;而实际上包括替加环素在内的四环素类药物对铜绿假单胞菌都不太敏感。此外,依拉环素的组织穿透性强,其肺部、血浆暴露量是替加环素的2倍,对不同部位感染的治疗均有优势。
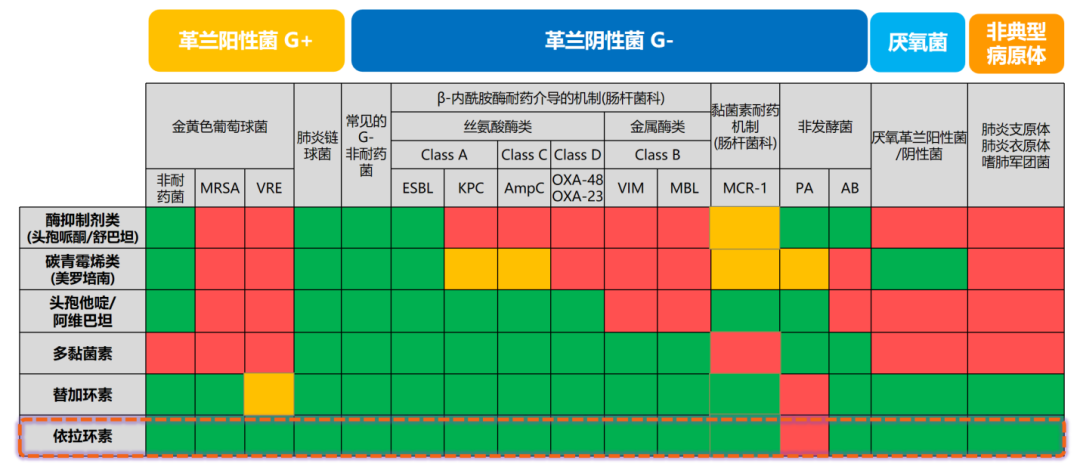
△体外抗菌活性显示,依拉环素可覆盖几乎所有常见致病菌,包括革兰阳性菌、革兰阴性菌(铜绿假单胞菌除外)、厌氧菌、非典型病原体[3]
“我认为依拉环素这类新药的加入对延缓其本身以及其他药物的耐药,一定会有很好的助推效应。临床医生对其上市可及也是持欢迎态度,希望能够尽快为临床所用。”卓超教授最后总结道。

施毅 教授
ICU是耐药“重灾区”
经验性治疗需要科学研判和分层
近年来,全球细菌耐药问题依然严峻,尤其是碳青霉烯类耐药革兰阴性杆菌(CRO)的耐药检出率居高不下。重症监护室(ICU)是反映细菌耐药趋势的重要窗口,也是细菌耐药的“重灾区”。施毅教授指出,重症患者的宿主免疫功能较差、暴露感染的风险较高,可出现不同部位、不同系统的耐药菌感染,尤其呼吸道是开放系统,ICU耐药菌感染率较高。从近年来的监测数据来看,尽管早些时候通过限制抗菌药使得CRO检出率略有下降趋势,但随着时间延长又趋于平缓甚至有抬头趋势。因此,细菌耐药问题无法仅靠限制用药得到完全解决,需要采取综合措施。
在谈到如何进行合理用药时,施毅教授认为,已经明确病原的目标治疗相对容易,难是难在如何进行合理的经验治疗,这是一门兼顾提高治疗成功率和减少药物滥用的临床“艺术”。经验治疗需要建立在全面评估、结合循证的基础上。施毅教授表示,我们反对没有分析判断的经验治疗,把经验治疗误解为“老师怎么说的,我曾经怎么做的……”合理的经验治疗,需要结合本科室、医院和当地的病原菌流行病学特征,对患者进行个体化的病情评估,包括感染部位、影像学表现、实验室检查结果、患者病情(例如合并症、免疫功能状态、既往抗菌药使用情况、有无细菌定植/感染病史等)等,在没有获得病原学诊断和药敏结果之前,初步判断可能的耐药菌感染类型,抗菌药选择时才能有的放矢;而且在治疗过程中,需要根据病情进展和其他检查结果进行治疗方案的动态调整、修正。随着实践经验的积累以及临床研究的丰富,我们也会有更多分层的危险因素,为耐药菌感染的经验治疗提供参考。
对于如何进行CRO感染的治疗和控制,施毅教授表示,一方面是通过合理用药,延长抗菌药的使用寿命;另一方面是加快创新药物的研发,为临床提供新的治疗“武器”。例如,第二代四环素类药物(如多西环素、米诺环素)问世后,大约间隔30多年才有了第三代替加环素的上市,几乎是两代人才看到一个新药问世。但替加环素进入中国仅10余年,随着药品使用的增加,其最低抑菌浓度值(MIC)越来越高,临床应用的有效剂量增加,意味着患者不良反应和细菌耐药性的风险增加。新型全合成含氟四环素依拉环素的问世,为院内获得性感染提供了更加有力的治疗“武器”。依拉环素对很多菌种的MIC都很低,抗菌活性更强;且同时组织浓度高,其肺部、血浆暴露量是替加环素的2倍,且针对肠杆菌和MRSA,其AUC/MIC也是替加环素的2~4倍,即便是严重耐药或替加环素治疗效果不好的细菌感染,也有很好的治疗效果。
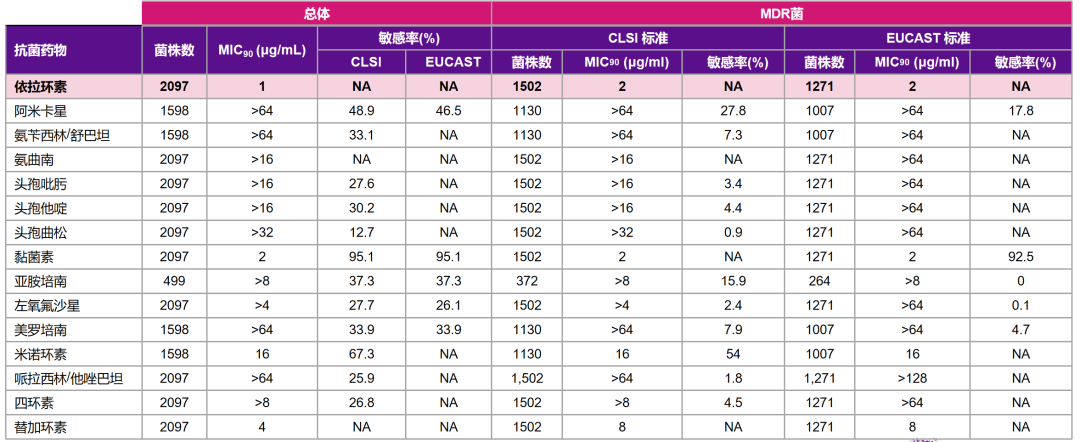
△全球药敏数据(2013-2017)显示,依拉环素对包括鲍曼不动杆菌(包括多重耐药)的MIC90相较替加环素低4倍[4]
施毅教授认为:“依拉环素的上市,很大程度上可以缓解革兰阴性耐药菌感染问题,尤其是在CRO治疗中发挥重要作用。目前的循证医学证据支持依拉环素疗效和安全性的优势,希望该药物尽快进入我国临床实践,成为我们应对耐药菌感染的新武器。”

郑波 教授
依拉环素联合用药
治疗常见CRO有良好的协同效应
革兰阴性菌是临床最常见的感染病原菌,其耐药性问题受到广泛关注。根据全国细菌耐药监测网(CARSS)报告的数据,2021年全国监测的革兰阴性菌感染占71.1%。尤其是CRO检出率整体上仍然居高不下甚至有抬头趋势。例如,2021年碳青霉烯耐药鲍曼不动杆菌(CR-ABA)检出率为54.3%,较上一年上升了0.6个百分点,仍然维持较高的水平;碳青霉烯类耐药肺炎克雷伯菌(CR-KPN)检出率为11.3%,较上一年上升了0.4个百分点[5]。
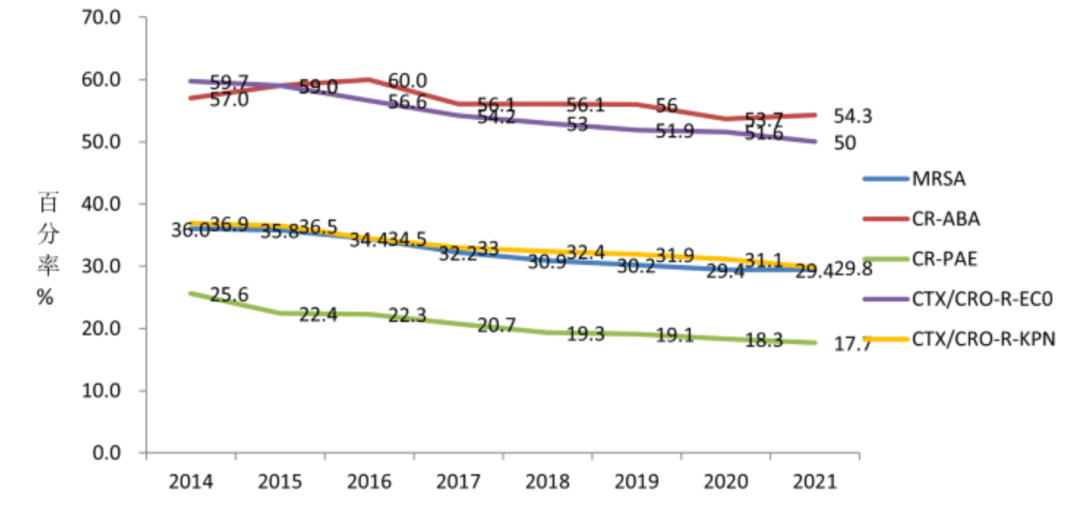
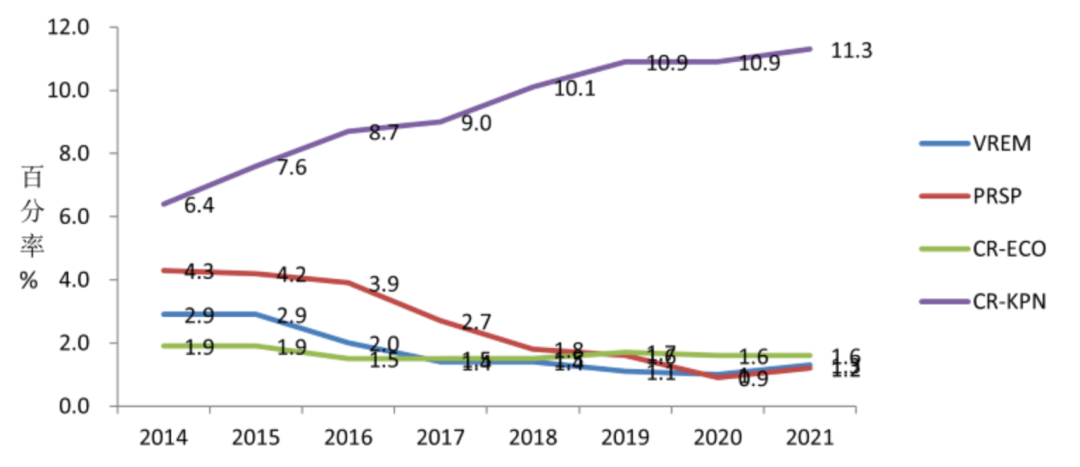
△2021年CARSS监测数据:全国特殊与重要耐药细菌检出率[5]
CRO检出率增加也为临床治疗带来挑战。近年来较为提倡的抗菌药治疗策略是,通过多药联合治疗而延长抗菌药物的使用寿命,已有体外联合药敏试验证实两药呈协同或相加作用的联合,能有效改善CRO感染患者的病死率。那么,作为新型的、广谱的、全合成含氟四环素类抗菌药,依拉环素联合用药能否增加药物敏感性?郑波教授团队开展的一项研究[6],对60株CRO进行药敏试验,以评估拉环素联合治疗的抗菌活性。
研究结果显示,依拉环素对碳青霉烯类耐药性大肠埃希菌、肺炎克雷伯菌、鲍曼不动杆菌的MIC50和MIC90均较低(大约在1mg/L左右),敏感性在85%~100%(下图左);而且依拉环素联合不同抗菌药,针对碳青霉烯类耐药大肠埃希菌、肺炎克雷伯菌、鲍曼不动杆菌的均可产生协同效应,尤其是依拉环素+多黏菌素B治疗碳青霉烯类耐药大肠埃希菌(协同率35%),依拉环素+多黏菌素B治疗碳青霉烯类耐药性肺炎克雷伯菌(协同率35%),依拉环素+亚胺培南(协同率55%)或依拉环素+头孢他啶(协同率70%)治疗碳青霉烯类耐药鲍曼不动杆菌均有较为理想的协同作用(下图右)。
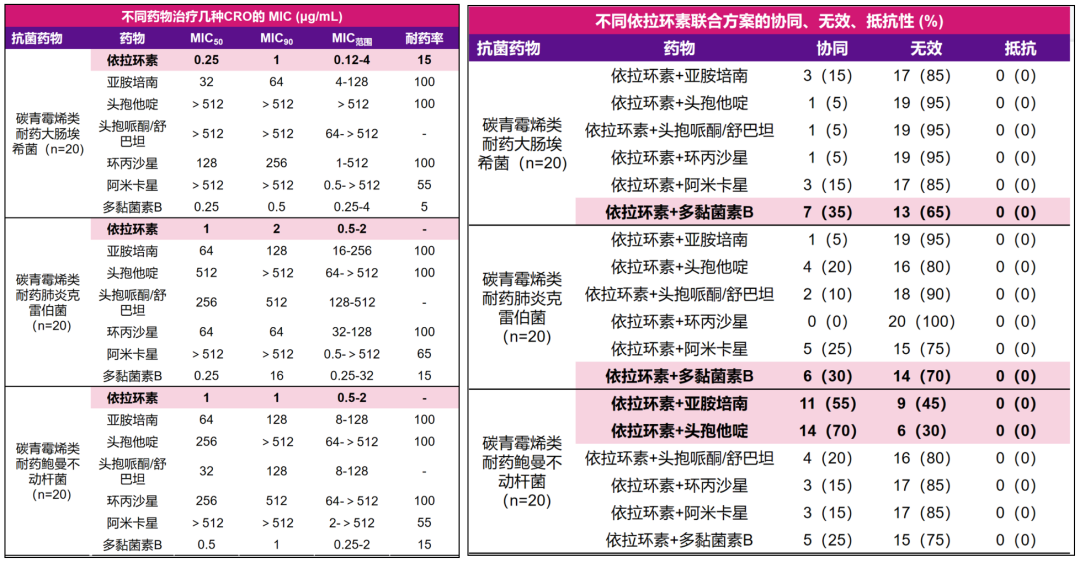
△不同抗菌药物治疗碳青霉烯类耐药性大肠埃希菌、肺炎克雷伯菌、鲍曼不动杆菌的最低抑菌浓度(MIC),以及不同依拉环素联合方案的协同率[6]
该研究结果表明,依拉环素单药或联合用药对临床常见CRO的抗菌活性较高,且联合用药可产生良好的协同作用。郑波教授表示:“根据已有的药物PK/PD特征、体外药敏和联合药敏结果,以及目前已经积累的循证医学证据,依拉环素这一类药物的安全性好、抗菌谱广、抗菌活性高,将为临床提供非常好的抗感染治疗武器,有很好的应用前景。”
参考文献
[1]Antimicrobial Resistance Collaborators. Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis [published correction appears in Lancet. 2022 Oct 1;400(10358):1102]. Lancet. 2022;399(10325):629-655.
[2]Tamma PD, Aitken SL, Bonomo RA, Mathers AJ, van Duin D, Clancy CJ. Infectious Diseases Society of America Guidance on the Treatment of Extended-Spectrum β-lactamase Producing Enterobacterales (ESBL-E), Carbapenem-Resistant Enterobacterales (CRE), and Pseudomonas aeruginosa with Difficult-to-Treat Resistance (DTR-P. aeruginosa). Clin Infect Dis. 2021;72(7):e169-e183.
[3]Alosaimy S, Abdul-Mutakabbir JC, Kebriaei R, Jorgensen SCJ, Rybak MJ. Evaluation of Eravacycline: A Novel Fluorocycline. Pharmacotherapy. 2020;40(3):221-238.
[4]Morrissey I, Olesky M, Hawser S, et al. In Vitro Activity of Eravacycline against Gram-Negative Bacilli Isolated in Clinical Laboratories Worldwide from 2013 to 2017. Antimicrob Agents Chemother. 2020;64(3):e01699-19. Published 2020 Feb 21.
[5]2021年全国细菌耐药监测报告.From:https://mp.weixin.qq.com/s/CXgJpXYH05G8MhixBS-P6Q
[6]Li Y, Cui L, Xue F, Wang Q, Zheng B. Synergism of eravacycline combined with other antimicrobial agents against carbapenem-resistant Enterobacteriaceae and Acinetobacter baumannii. J Glob Antimicrob Resist. 2022;30:56-59.
(来源:《感染医线》)
声 明
凡署名原创的文章版权属《感染医线》所有,欢迎分享、转载(开白可后台留言)。本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。

责任编辑:彭伟彬
相关搜索: CRO